పొడి కణం విద్యుత్ ఉత్పత్తి చేసే మూలం యొక్క సరళమైన రూపం. అనేక కణాలు కలిపి కణాలు కలిసి బ్యాటరీని ఏర్పరుస్తాయి. ది సీసం-ఆమ్లం లేదా నికెల్-కాడ్మియం బ్యాటరీ పొడి కణం యొక్క అధునాతన వెర్షన్. ఈ కణాన్ని మొట్టమొదట 1866 లో ఫ్రెంచ్ ఇంజనీర్ జార్జెస్ లెక్లాంచె కనుగొన్నారు. అతని ఆవిష్కరణకు అతని పేరును లెక్లాంచె బ్యాటరీ అని పేరు పెట్టారు. కానీ ఆ సమయంలో, ఇది చాలా భారీగా ఉంది మరియు సులభంగా విచ్ఛిన్నం కావచ్చు. పొడి కణం అదే సూత్రాన్ని కలిగి ఉంది మరియు ఇది లెక్లాంచ్ బ్యాటరీ యొక్క అధునాతన వెర్షన్ మరియు వివిధ వోల్టేజ్ మరియు పరిమాణాలలో వస్తుంది. జింక్-కార్బన్ సెల్ యొక్క వాణిజ్య రూపం, ఇది లెక్లాంచ్ బ్యాటరీ యొక్క సవరించిన రూపం, 1881 లో మెయిన్జ్ యొక్క కార్ల్ గాస్నర్ చేత కనుగొనబడింది. ఇది గొప్ప పరిమాణంలో ఉత్పత్తి చేయబడుతుంది మరియు బొమ్మలు, రేడియోలు, కాలిక్యులేటర్లు మొదలైన అనేక అనువర్తనాలలో ఉపయోగించబడుతుంది.
డ్రై సెల్ అంటే ఏమిటి?
పొడి కణం రసాయన ప్రతిచర్యల ఆధారంగా విద్యుత్తును ఉత్పత్తి చేసే పరికరం. కణం యొక్క రెండు ఎలక్ట్రోడ్లు క్లోజ్డ్ మార్గం ద్వారా అనుసంధానించబడినప్పుడు, అప్పుడు సెల్ ఎలక్ట్రాన్లను ఒక చివర నుండి మరొక చివర వరకు ప్రవహిస్తుంది. ఎలక్ట్రాన్ల ప్రవాహం క్లోజ్డ్ సర్క్యూట్లో ప్రవాహాన్ని ప్రవహిస్తుంది.

డ్రై సెల్ పొరలు
రసాయన ప్రతిచర్యల సహాయంతో, ఎలక్ట్రాన్లు ఒక చివర నుండి మరొక చివర వరకు ప్రవహిస్తాయి. రెండు లేదా అంతకంటే ఎక్కువ కణాలు, సరైన ధ్రువణతతో అనుసంధానించబడినప్పుడు, అధిక సామర్థ్యం కారణంగా ఎక్కువ ఎలక్ట్రాన్లు ప్రవహిస్తాయి. ఈ కలయికను బ్యాటరీ అంటారు. కనీస వోల్టేజ్ 1.5 V నుండి 100 V వరకు, వోల్టేజీల శ్రేణిని పొందడానికి బ్యాటరీని ఉపయోగించవచ్చు. బ్యాటరీ యొక్క అవుట్పుట్ DC వోల్టేజ్ కూడా పవర్ ఎలక్ట్రానిక్ కన్వర్టర్లను ఉపయోగించి వివిధ స్థాయిలకు నియంత్రించవచ్చు ఛాపర్ సర్క్యూట్లు.
సెల్ యొక్క నిర్మాణం
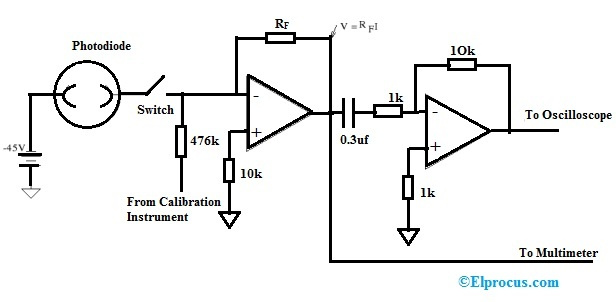
జింక్-కార్బన్ డ్రై సెల్ యొక్క నిర్మాణం చిత్రంలో చూపబడింది. ఇది యానోడ్ టెర్మినల్ను జింక్ లేదా సాధారణ గ్రాఫైట్ రాడ్లో కలిగి ఉంటుంది. కార్బన్ కాథోడ్ టెర్మినల్ను ఏర్పరుస్తుంది. పొడి కణం యొక్క పాత వెర్షన్లలో జింక్ను కాథోడ్గా మరియు గ్రాఫైట్ను యానోడ్ టెర్మినల్గా ఉపయోగించడాన్ని గమనించవచ్చు. మూలకాల ఎంపిక ప్రాథమికంగా మూలకాల యొక్క బయటి కక్ష్య యొక్క రసాయన ఆకృతీకరణపై ఆధారపడి ఉంటుంది.

డ్రై సెల్ నిర్మాణం
బయటి కక్ష్యలో ఎక్కువ సంఖ్యలో ఎలక్ట్రాన్లు ఉంటే, అది దాతగా పనిచేస్తుంది, అందువల్ల కాథోడ్ ఏర్పడుతుంది. అదేవిధంగా, బయటి కక్ష్యలో తక్కువ ఎలక్ట్రాన్లు ఉంటే, అది సులభంగా అంగీకరించగలదు మరియు అందువల్ల యానోడ్ను ఏర్పరుస్తుంది. మధ్యలో ఉంచిన ఎలక్ట్రోలైట్ రసాయన ప్రతిచర్యలకు ఉత్ప్రేరకంగా పనిచేస్తుంది. సాధారణంగా, మేము అమ్మోనియం క్లోరైడ్ జెల్లీని ఎలక్ట్రోలైట్గా ఉపయోగిస్తాము. చూపిన చిత్రంలో, ఉపయోగించిన ఎలక్ట్రోలైట్ జింక్ మరియు క్లోరైడ్ మిశ్రమం. అలాగే, సోడియం క్లోరైడ్ను ఎలక్ట్రోలైట్గా కూడా ఉపయోగిస్తారు. మాంగనీస్ డయాక్సైడ్ మరియు కార్బన్ మిశ్రమం యానోడ్ రాడ్ చుట్టూ ఉంది.
మొత్తం కాన్ఫిగరేషన్ మెటల్ ట్యూబ్లో ఉంచబడుతుంది. సెల్ పైభాగంలో పిచ్ ఉపయోగించడం ద్వారా జెల్లీ ఎండిపోకుండా నిరోధించబడుతుంది. కార్బన్ వాషర్ దిగువన ఉంచబడుతుంది. ఈ ఉతికే యంత్రం యొక్క ఉద్దేశ్యం జింక్ యానోడ్ రాడ్ కంటైనర్తో సంబంధంలోకి రాకుండా నిరోధించడం.
రేఖాచిత్రంలో చూపిన విధంగా దీనిని స్పేసర్ అని కూడా పిలుస్తారు. జింక్ డబ్బా కూడా ఇన్సులేషన్ ప్రయోజనాల కోసం కాగితం ఇన్సులేషన్ ద్వారా ఉంటుంది. పెద్ద బ్యాటరీల కోసం, మైకా మొదలైన ఇతర ఇన్సులేటింగ్ పదార్థాలను కూడా ఉపయోగిస్తారు. ఎల్ యొక్క సానుకూల టెర్మినల్ ఎగువన ఏర్పడుతుంది. సెల్ యొక్క ప్రతికూల టెర్మినల్ బేస్ వద్ద ఏర్పడుతుంది.
డ్రై సెల్ యొక్క పని
పొడి కణం ప్రాథమికంగా రసాయన ప్రతిచర్యలపై పనిచేస్తుంది. ఎలక్ట్రోలైట్ మరియు ఎలక్ట్రోడ్ల మధ్య జరిగే ప్రతిచర్యల కారణంగా, ఎలక్ట్రాన్లు ఒక ఎలక్ట్రోడ్ నుండి మరొకదానికి ప్రవహిస్తాయి. ఆమ్లాలు వంటి పదార్థాలు నీటిలో కరిగి అయనీకరణ కణాలు ఏర్పడతాయి. అయోనైజ్డ్ కణం రెండు రకాలు. సానుకూల అయాన్లను కాటయాన్స్ మరియు ప్రతికూల అయాన్లను అయాన్లు అంటారు. నీటిలో కరిగే ఆమ్లాలను ఎలక్ట్రోలైట్స్ అంటారు.
పైన పేర్కొన్న రేఖాచిత్రంలో, జింక్ క్లోరైడ్ ఎలక్ట్రోలైట్గా ఏర్పడుతుంది. అదేవిధంగా అమ్మోనియం క్లోరైడ్ జెల్లీ కూడా ఎలక్ట్రోలైట్గా ఏర్పడుతుంది. ఎలక్ట్రోలైట్లలో మునిగిపోయిన లోహపు కడ్డీలు ఎలక్ట్రోడ్లను ఏర్పరుస్తాయి. లోహపు కడ్డీల యొక్క రసాయన లక్షణాల ఆధారంగా, మనకు సానుకూల ఎలక్ట్రోడ్ యానోడ్ మరియు కాథోడ్ వలె ప్రతికూల ఎలక్ట్రోడ్ ఉన్నాయి.
ఎలక్ట్రోడ్లు వ్యతిరేక చార్జ్ చేసిన అయాన్లను వాటి వైపుకు ఆకర్షిస్తాయి. ఉదాహరణకు, కాథోడ్ అయాన్లను ఆకర్షిస్తుంది మరియు యానోడ్ కాటయాన్ను ఆకర్షిస్తుంది. ఈ ప్రక్రియలో ఎలక్ట్రాన్లు ఒక దిశ నుండి మరొక వైపుకు ప్రవహిస్తాయి, అందువల్ల మనకు ఛార్జీల ప్రవాహం లభిస్తుంది. దీనిని అంటారు ప్రస్తుత .
రసాయన ప్రతిచర్యలు
కణంలో జరుగుతున్న ప్రతిచర్యలు క్రింద చూపించబడ్డాయి. మొదటిది ఆక్సీకరణ చర్య.

దీనిలో, జింక్ కాథోడ్ రెండు అయాన్లను విడుదల చేసే ధనాత్మక చార్జ్ చేసిన జింక్ అయాన్లకు ఆక్సీకరణం చెందుతుంది. ఈ ఎలక్ట్రాన్లు యానోడ్ చేత సేకరించబడతాయి. అప్పుడు తగ్గింపు ప్రతిచర్య వస్తుంది.

యానోడ్ వద్ద తగ్గింపు ప్రతిచర్య పైన చూపబడింది. ఈ ప్రతిచర్య విద్యుత్ ప్రవాహాన్ని ఉత్పత్తి చేస్తుంది. ఇది మెగ్నీషియం ఆక్సైడ్తో ఆక్సైడ్ అయాన్లను విడుదల చేస్తుంది. మెగ్నీషియం ఎలక్ట్రోలైట్తో కలిపినప్పుడు ఈ ప్రతిచర్య ఏర్పడుతుంది.


ఇతర రెండు ప్రతిచర్యలు పొడి కణంలో జరుగుతున్న యాసిడ్-బేస్ ప్రతిచర్య మరియు అవపాత ప్రతిచర్యను సూచిస్తాయి. యాసిడ్-బేస్ ప్రతిచర్యలో, NH ను OH తో కలిపి నీటితో పాటు NH3 ను ఉత్పత్తి చేస్తుంది. ఫలితాలు NH3 మరియు నీటి స్థావరం.
డ్రై సెల్ మరియు వెట్ సెల్ మధ్య తేడా
పొడి కణం మరియు తడి కణం మధ్య ప్రధాన వ్యత్యాసం ఎలక్ట్రోలైట్ యొక్క రూపం. ముందు చర్చించినట్లుగా, పొడి కణంలో, అమ్మోనియం క్లోరైడ్ వంటి ఎలక్ట్రోలైట్ ప్రకృతిలో పొడిగా ఉంటుంది. ఇటువంటి పొడి కణాలు ఎక్కువగా కనిపిస్తాయి మరియు బొమ్మలు, రేడియోలు మొదలైన వాటిలో ఉపయోగిస్తారు. కాని తడి కణంలో ఎలక్ట్రోలైట్ ద్రవ స్థితిలో ఉంటుంది.
ప్రమాదకరమైన తినివేయు ద్రవమైన సల్ఫ్యూరిక్ ఆమ్లం వంటి ద్రవ ఎలక్ట్రోలైట్లను ఉపయోగిస్తారు. అటువంటి ద్రవాల స్వభావం కారణంగా, తడి కణం ప్రకృతిలో మరింత పేలుడుగా ఉంటుంది మరియు జాగ్రత్తగా నిర్వహించాల్సిన అవసరం ఉంది. అటువంటి తడి కణాల యొక్క ఉత్తమ ప్రయోజనం ఏమిటంటే అవి సులభంగా రీఛార్జ్ చేయబడతాయి మరియు అనేక అనువర్తనాలకు ఉపయోగించబడతాయి. ఇటువంటి బ్యాటరీలు విమానయానం, యుటిలిటీస్, ఎనర్జీ స్టోరేజ్ మరియు సెల్ ఫోన్ టవర్లలో సాధారణ వాడకాన్ని కనుగొంటాయి.
డ్రై సెల్ విధులు
ఎలక్ట్రోడ్ మరియు ఎలక్ట్రోలైట్ల మధ్య రసాయన ప్రతిచర్యల ఆధారంగా పొడి కణాల పనితీరు. ఎలక్ట్రోడ్లను ఎలక్ట్రోలైట్లలో ఉంచినప్పుడు, అది తమ వైపుకు వ్యతిరేక చార్జ్ అయాన్లను ఆకర్షిస్తుంది. ఇది ఛార్జీల ప్రవాహానికి కారణమవుతుంది మరియు అందువల్ల కరెంట్ ఉత్పత్తి అవుతుంది.
ప్రయోజనాలు
ది పొడి కణం యొక్క ప్రయోజనాలు కింది వాటిని చేర్చండి.
- పొడి కణం వంటి అనేక ప్రయోజనాలు ఉన్నాయి
- ఇది పరిమాణంలో చిన్నది.
- ఇది రకరకాల వోల్టేజ్ స్థాయిలలో రావచ్చు.
- ఇది సులభ మరియు అనేక అనువర్తనాలను కలిగి ఉంది.
- ఇది DC వోల్టేజ్ యొక్క ఏకైక మూలం.
- అవుట్పుట్ వోల్టేజ్ను నియంత్రించడానికి పవర్ ఎలక్ట్రానిక్ సర్క్యూట్లతో పాటు దీనిని ఉపయోగించవచ్చు
- ఇది పునర్వినియోగపరచదగినది.
ప్రతికూలతలు
ది పొడి కణం యొక్క ప్రతికూలతలు కింది వాటిని చేర్చండి.
- దీన్ని జాగ్రత్తగా నిర్వహించాలి
- ఇది పేలుడు
- పెద్ద రేటింగ్ బ్యాటరీలు చాలా భారీగా ఉంటాయి
అప్లికేషన్స్
ది పొడి కణం యొక్క అనువర్తనాలు కింది వాటిని చేర్చండి.
- బొమ్మలు
- విమానయానం
- సెల్ ఫోన్లు
- రేడియో
- కాలిక్యులేటర్
- గడియారాలు
- వినికిడి పరికరాలు
అందువల్ల మేము ఆపరేషన్, వర్గీకరణ మరియు అనువర్తనాలను చూశాము పొడి కణాలు . గమనించదగ్గ ఒక ఆసక్తికరమైన విషయం ఏమిటంటే, ఎలక్ట్రోడ్లు భౌతికంగా ఒకదానితో ఒకటి సన్నిహితంగా ఉన్నప్పుడు మాత్రమే బ్యాటరీ పనిచేస్తుంది. రెండు ఎలక్ట్రోడ్ల మధ్య ఒక వాహక మాధ్యమం ఉండాలి. పొడి కణం యొక్క ఎలక్ట్రోడ్ల మధ్య నీటిని వాహక మాధ్యమంగా ఉపయోగించవచ్చా అనేది ప్రశ్న. అలాంటప్పుడు, ఈ కణాన్ని నీటిలో ముంచితే ఏమి జరుగుతుంది?